Tercera Ley de Newton
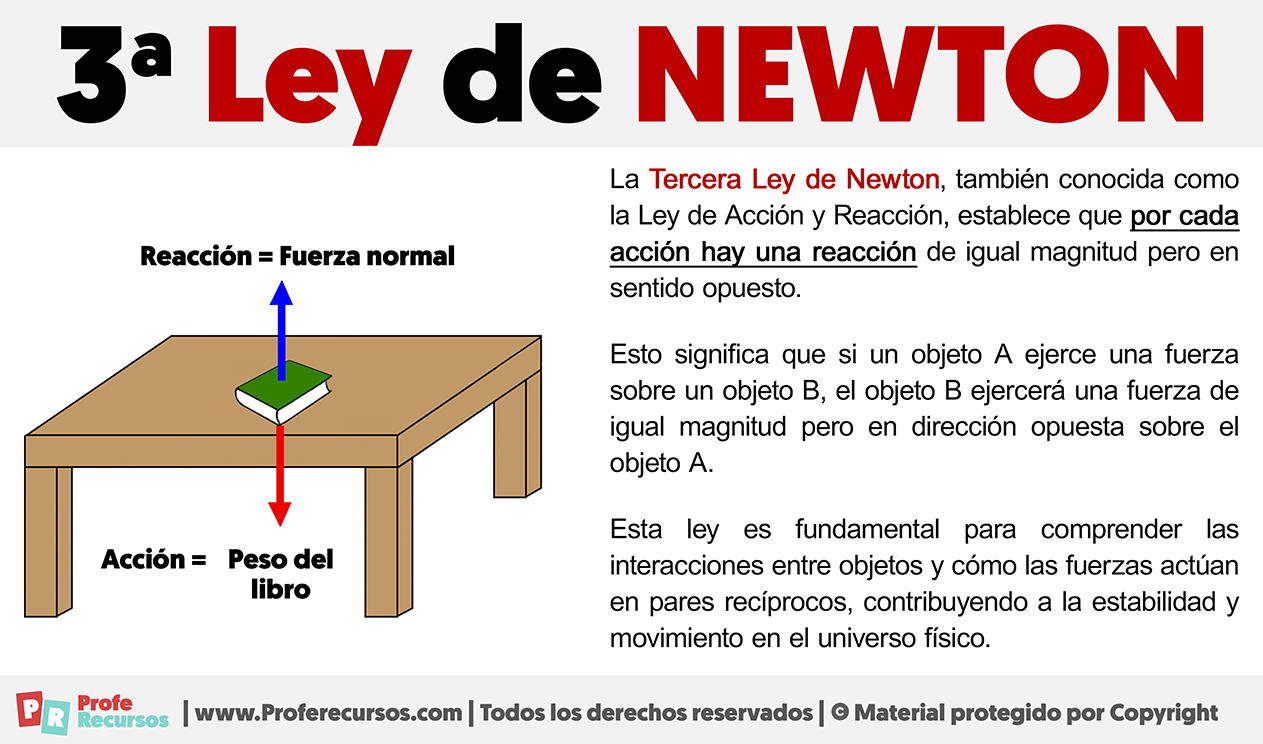
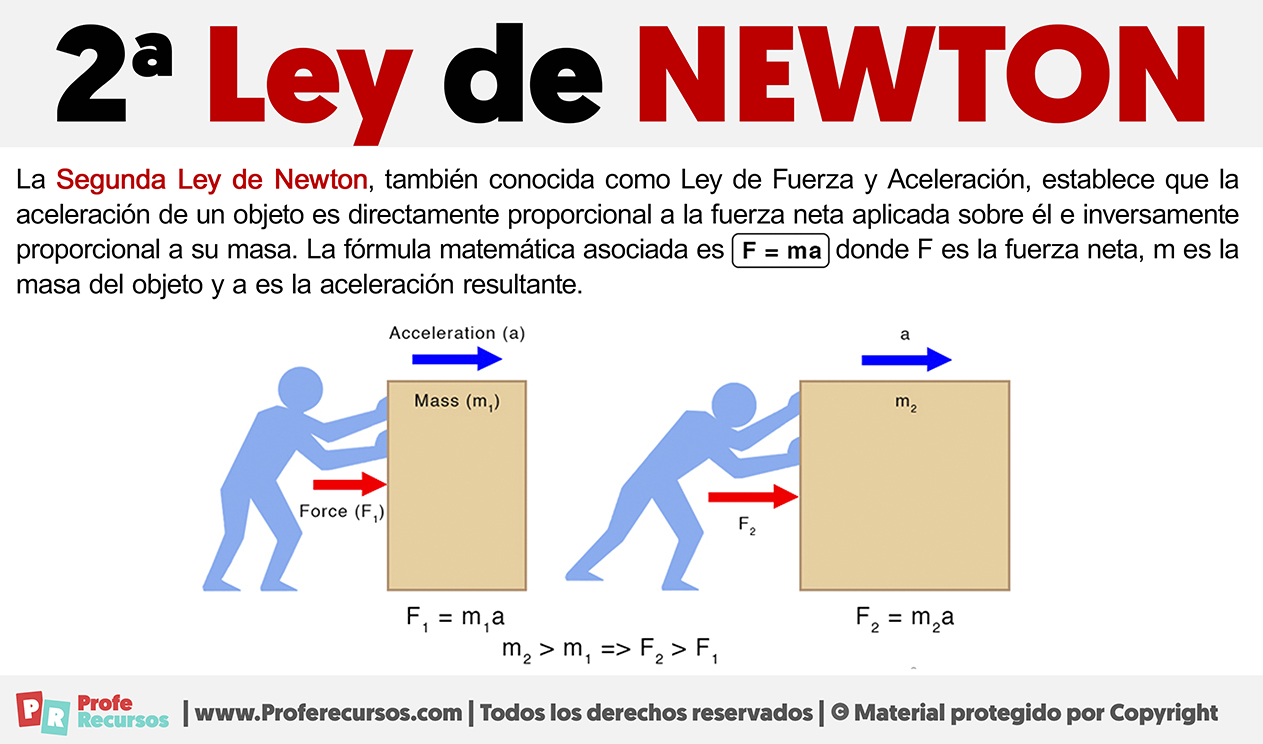
La Tercera Ley de Newton, también conocida como la Ley de Acción y Reacción, establece que por cada acción hay una reacción de igual magnitud pero en sentido opuesto. Esto significa que si un objeto A ejerce una fuerza sobre un objeto B, el objeto B ejercerá una fuerza de igual magnitud pero en dirección opuesta sobre el objeto A. Esta ley es fundamental para comprender las interacciones entre objetos y cómo las fuerzas actúan en pares recíprocos, contribuyendo a la estabilidad y movimiento en el universo físico. Ejemplos de aplicación de la 3ª Ley de Newton Veamos algunos ejemplos donde podemos aplicar la Ley de Acción y Reacción: Ejemplo 1: Cohetes en el Espacio La tercera ley de Newton establece que por cada acción hay una reacción igual y opuesta. En el caso de los cohetes, la expulsión de gases a alta velocidad hacia atrás genera una fuerza de reacción hacia adelante, propulsando al cohete en el espacio. Ejemplo 2: Salto de un Trampolín Cuando una persona salta en un [...]